中国药企等摸索免疫细胞治疗固体癌
2022/02/24
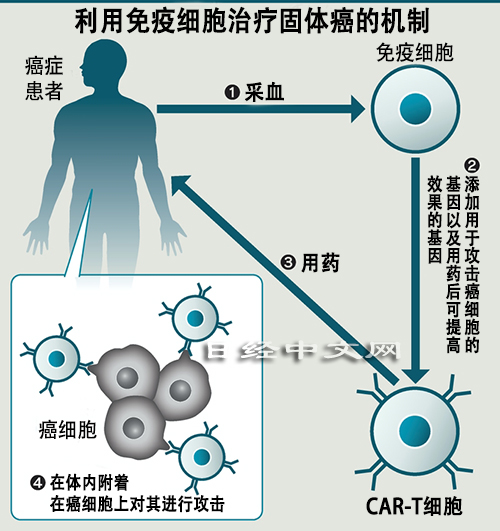
针对在癌症中占比超过9成的固体癌(Solid Cancer),继手术、放射线、抗癌剂、免疫药物之后,又出现了新的治疗方法。这种新方法使用改变基因的免疫细胞,改进了在血癌治疗中实现实用化的免疫疗法。中国的初创企业计划2023年向美国食品药品监督管理局(FDA)申请生产销售许可证,美国企业和日本武田药品工业也在加紧进行临床试验。
 |
全球每年新增癌症患者的人数约两千万人,其中约一半人死亡。在每年超过5千万的总死亡人数中,约占六分之一。今后,随着人口的增加和寿命的延长,老年阶层将会扩大,预计罹患癌症的人数还会增加。
据美国调查公司BCC Research预测,到2026年全球癌症治疗药物市场规模将达到3137亿美元,比2021年扩大77%。其中绝大部分是用于患者人数较多的肺癌及大肠癌等固体癌的药物。
 |
| 日本BrightPath Biotherapeutics计划针对骨软骨瘤和固体癌实施采用CAR-T疗法的临床试验(图片由该公司提供) |
癌症目前的主要治疗方法是手术、放射线、抗癌剂和免疫药物。但手术无法切除的转移性癌症等很难通过放射线和抗癌剂治愈。2010年代开始使用的免疫药物也很难治疗胰脏癌等棘手癌症和晚期癌症。目前,针对白血病等血癌,被称为CAR-T的疗法具有治疗效果,对该疗法进行改进之后实施的临床试验也正接连不断地展开。
中国医药初创企业科济生物医药(CARsgen Therapeutics)利用从患者的血液中提取的免疫细胞制作出了CAR-T细胞。该CAR-T细胞通过向患者的免疫细胞植入可生成用于攻击癌细胞的CAR蛋白质的基因而制成。该公司还进一步开发出了增强疗效的方法。在CAR-T细胞中还追加植入了可生成附着在胃癌和胰脏癌等癌细胞上的蛋白质的基因,从而使CAR-T细胞更容易追踪和攻击容易转移的癌细胞。
科济生物已在中国完成针对胃癌的第一阶段临床试验,目前正在计划实施第二阶段临床试验。该公司目前还在美国推进第一阶段临床试验,预定于2023年申请生产销售许可证。由于该药被FDA和欧洲药品管理局(EMA)指定为罕见病药物,如果临床试验能够证实其效果,将有望在2023年以后上市。
版权声明:日本经济新闻社版权所有,未经授权不得转载或部分复制,违者必究。
报道评论
HotNews
金融市场
| 日经225指数 | 64179.27 | -1237.36 | 06/10 | close |
| 日经亚洲300i | 3194.54 | -93.82 | 06/10 | close |
| 美元/日元 | 160.54 | 0.16 | 06/11 | 08:15 |
| 美元/人民元 | 6.7717 | -0.0003 | 06/11 | 00:13 |
| 道琼斯指数 | 49918.78 | -953.33 | 06/10 | close |
| 富时100 | 10254.810 | 27.480 | 06/10 | close |
| 上海综合 | 3993.2258 | -16.8049 | 06/10 | close |
| 恒生指数 | 24407.96 | -157.94 | 06/10 | close |
| 纽约黄金 | 4108.2 | -151.8 | 06/10 | close |







