新冠口服药最快年内问世,用药方便易于量产
2021/09/24
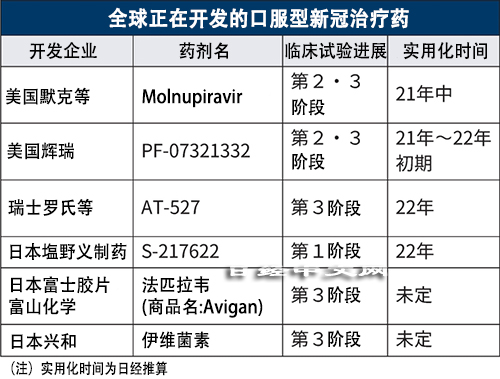
治疗新冠病毒的口服药有望最早在年内问世。美国两家药企默克(Merck)和辉瑞(Pfizer)正在包括日本在内的各国推进能用于轻症者的药剂的最终阶段临床试验。与点滴注射型的现有新冠治疗药相比除了更容易用药外,还易于推进量产,更能降低成本。因此,新冠口服药被期待能推动疫情的全球大流行走向平息。
 |
| 美国药企默克的抗病毒药“Molnupiravir”(图由该公司提供) |
默克正携手美国新兴企业Ridgeback Biotherapeutics开发抗病毒药“Molnupiravir”。目前正在全球范围推进临床试验,相关数据被认为最早将在10月公开。默克方面还透露了2021年内在美国申请紧急使用许可的计划。有可能在此之后的1~2个月后在日本申请特例批准。
这款抗病毒药原本用于流感的治疗,但被认为对新冠病毒也同样有效。美国卫生与社会福利部(HHS)已经与默克签署了以12亿美元采购170万剂的合同。默克正在推进量产准备工作,力争到2021年底生产1000万剂。
 |
美国辉瑞也在研发同样的抗病毒药。通过改进2002~2003年面向"非典"(重症急性呼吸综合征、SARS)而开发的药物,正在开发静脉注射型和口服型等2种新冠治疗药。相关药物将并未入院的轻症到中等症状的患者作为对象。辉瑞透露了2021年10~12月内发布初步数据的计划,有望早日实现实用化。
美国的紧急使用许可是在生物恐怖袭击等非常时期临时允许未批准药等使用的制度,本来需要半年至1年的审查时间被缩短至3周左右。与正式批准不同,在安全性和有效性不充分的情况下,也有可能取消批准。
日本也具有特例批准制度,针对美国和英国等存在与日本相同水平药品审查标准的海外使用的药品,在非常时期作为特例给予正式批准,允许进口。通常情况下需要半年至近1年的审查时间缩短至2个月左右。
版权声明:日本经济新闻社版权所有,未经授权不得转载或部分复制,违者必究。
HotNews
金融市场
| 日经225指数 | 64179.27 | -1237.36 | 06/10 | close |
| 日经亚洲300i | 3194.54 | -93.82 | 06/10 | close |
| 美元/日元 | 160.52 | 0.14 | 06/11 | 08:42 |
| 美元/人民元 | 6.7718 | -0.0002 | 06/11 | 00:42 |
| 道琼斯指数 | 49918.78 | -953.33 | 06/10 | close |
| 富时100 | 10254.810 | 27.480 | 06/10 | close |
| 上海综合 | 3993.2258 | -16.8049 | 06/10 | close |
| 恒生指数 | 24407.96 | -157.94 | 06/10 | close |
| 纽约黄金 | 4108.2 | -151.8 | 06/10 | close |







