“万能细胞”向实用性临床试验迈进
2023/04/04
在以临床研究为主、可分化为所有细胞和组织的“万能细胞”领域,以实用化为目标的临床试验越来越多。继日本之后,住友制药(Sumitomo Pharma)2023年内将在美国启动用iPS细胞治疗帕金森病的临床试验。世界大型企业诺和诺德(Novo nordisk)将最早于2023年着手进行用胚胎干细胞(ES细胞)治疗帕金森病的临床试验。虽然仍存在很多课题,但澳大利亚企业已开始对患者较多的变形性骨关节炎进行最终临床试验等,目标是根治疑难病等。
 |
“iPS细胞是源自日本的技术,我们的使命是让使用这种细胞的再生医疗实现商业化,提供给更多患者”,住友制药社长野村博表示。住友制药计划2023年内在美国启动初期阶段临床试验,用iPS细胞治疗脑神经细胞发生异常的帕金森病。
帕金森病是运动功能出现异常导致麻木及肌肉僵硬等的疾病。据推算,到2030年,全世界的帕金森病患者人数将达到约1000万,但目前这种病还无法根治。在日本,2018年京都大学医院启动了由医生主导的临床试验,住友制药的目标是到2024年度在日本国内实现实用化。治疗方法是移植由iPS细胞制成的神经细胞,还将在帕金森患者人数较多的美国新设生产基地,为推广到全世界做准备。住友制药预计到2032年度再生医疗业务的年销售额将超过1千亿日元,在研究开发上共计投入了超过300亿日元的资金。
年内启动初期阶段临床试验
诺和诺德利用基于受精卵的ES细胞生成了可产生多巴胺的细胞。计划最早于2023年内在日美欧启动初期阶段临床试验,目标是将这种细胞移植到帕金森患者的脑部进行治疗。目前诺和诺德还在利用ES细胞生成可分泌胰岛素的细胞,推进用其治疗糖尿病的研究。诺和诺德首席执行官(CEO)周赋德(Lars Fruergaard Jrgensen)称,这种疗法“有望从根本上治愈糖尿病”。
 |
| 诺和诺德最早将于2023年内启动使用ES细胞的临床试验 |
安斯泰来(Astellas)制药也已进入用ES细胞治疗有可能导致失明的老年黄斑变性的初期临床试验阶段。
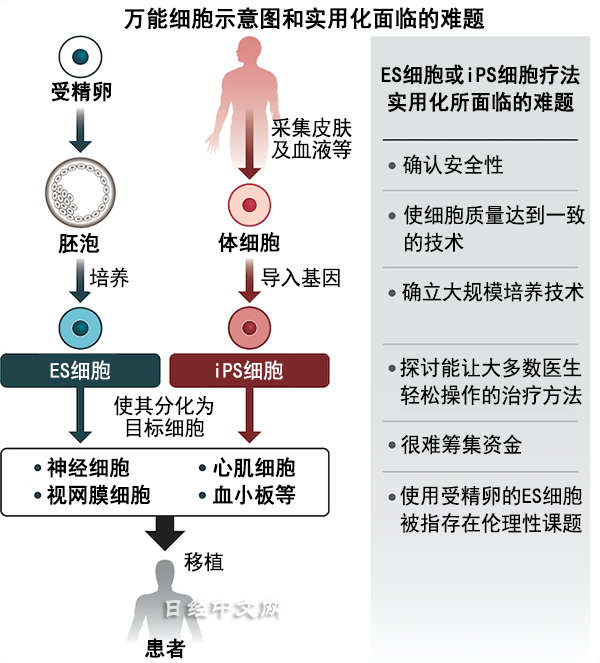
再生人体组织或器官、使其恢复功能的治疗技术统称为再生医疗。治疗手段广泛,也包括注入基因改造免疫细胞的治疗。虽然目前已出现用于重度烧伤患者的培养皮肤等已经获得批准的产品,但可转化为所有细胞的ES细胞和iPS细胞尚未得到实用化。
ES细胞方面,2010年美国生物制药企业杰龙(Geron)在全球首次临床试验中为脊髓损伤患者移植了用ES细胞生成的神经。iPS细胞是日本京都大学教授山中伸弥开发的技术,通过在皮肤等的细胞中导入基因来制备,2012年获得了诺贝尔生理学或医学奖。理化学研究所2014年对老年黄斑变性患者实施了全球首次临床研究。大阪大学在心脏病和眼角膜的临床研究领域走在前面,京都大学在帕金森等的临床研究方面处于领先地位。
随着全球临床研究的不断积累,在企业的参与下以获得批准和实现商业化为目标的临床试验越来越多。接近实用化的企业是澳大利亚Cynata Therapeutics。该公司以引发疼痛和功能障碍的变形性骨关节炎为对象,使用以iPS细胞制成的干细胞进行治疗,目前正在进行最后阶段的临床试验。美国有3000万名骨关节炎患者。
市场规模10年扩大至10倍
据理特咨询(Arthur D. Little)推测,到2030年,以候选新药为基础的“再生医疗与基因治疗”的全球市场规模将达到6.8万亿日元,10年时间扩大至约10倍,到2040年将达到12万亿日元。
但要实现实用化和普及,还需要解决包括确保安全性等在内的诸多课题。与化学合成药物不同,活体万能细胞很难在质量上达到一致。需要高效培养大量高品质的细胞,并掌握安全性确认技术。日本再生医疗学会理事长冈野荣之表示:“重要的是确立让医疗从业人员轻松进行安全管理和注射的方法”,还将考虑制定旨在保证治疗质量的医疗设施认定制度。
筹集资金也是一大难题。源自京都大学的初创企业Megakaryon于2022年启动了利用iPS细胞来治疗血小板减少状态的初期阶段临床试验。但在筹资方面遇到了困难,“虽然试验结果良好,但目前已中止临床试验”,Megakaryon表示。存在的课题是降低制造成本,Megakaryon正在大力开发可为更多患者输注的血小板制剂。
也有世界各国普遍采取货币紧缩政策的原因,2022年全球对再生医疗领域生物技术企业的投资比2021年减少了约4成。目前,缩减候选新药的制药企业越来越多,需要政企学联合对未来可期的候选新药采取培育措施。
日本在商业化上落后于人
理特咨询公司的统计显示,全世界已启动临床试验的“再生医疗与细胞治疗开发产品”共有836种(截止到2022年1月)。美国占5成,处于领先地位,欧洲不到2成,日本的占比还不到1成。美国在2020~2021年两年时间里增加了6成,呈现出加速趋势。
在欧美等海外国家,将改造基因的免疫细胞注入癌症患者体内的治疗用产品达到总体的7成。而日本则是“癌症以外的再生医疗”产品占8成,“日本正在医生的主导下追求(根治疑难病的)理想技术,美国则重视盈利性等,正在致力于治疗机制更加明确的领域”,理特咨询的花村辽指出。两个国家的倾向不同。
日本一直在iPS细胞的研究方面引领世界,但商业化步伐却落后于欧美国家。这10年来,日本政府为iPS细胞的实用化投入了1100亿日元资金,但这一政策将于3月底结束。目前距离临床试验、批准、稳定生产、研发再投资这一周期仍然很遥远。高品质细胞的稳定生产需要巨大的投资和人才投入。美国国立卫生研究院(NIH)每年向iPS细胞相关领域提供1000亿日元的资助。
美欧还在与再生医疗相关的基因治疗和基因组编辑方面拥有很多专利。日本的课题是建立相关机制,为政企学相结合的技术开发、商用制造和全球推广提供支持。
日本经济新闻(中文版:日经中文网)满武里奈
版权声明:日本经济新闻社版权所有,未经授权不得转载或部分复制,违者必究。
