阿尔茨海默病新药有何不同?
2021/06/09
据推算,全世界共有3千万阿尔茨海默型认知症患者,全球首款可抑制该病发展的药物将在美国投入使用。美国食品药品监督管理局(FDA)批准了美国渤健(Biogen)和日本卫材的新药“Aduhelm(Aducanumab)”。在药物需求高涨的背景下,FDA有条件地批准了这款新药。在日本,由于患者人数众多和价格昂贵,有人担心该药会挤压国家的医疗费用,新药获批成为备受关注的焦点。
据估算,全世界有5千万认知症患者,阿尔茨海默病是其中占比6成的主要疾病。这是一种进行性脑部疾病,记忆力和思考能力逐渐下降,最终导致日常生活陷入困难。
新药可清除致病物质
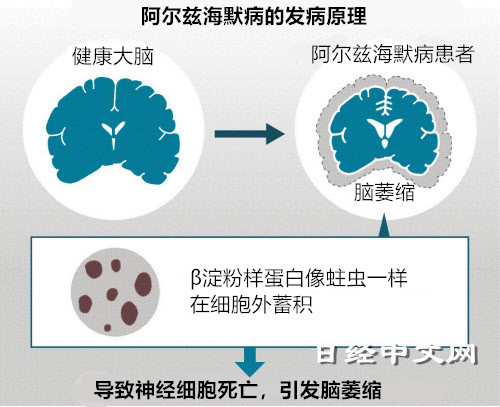
虽然阿尔茨海默病的发病原因尚不清楚,但已经查明的是,患者脑部蓄积了一种叫做“β淀粉样蛋白(amyloid-β)”的蛋白质,逐渐导致神经细胞受损,并最终造成脑萎缩。很多科学家和制药企业认为,只要清除淀粉样蛋白,就可以阻止病情的发展,因此一直在挑战可阻碍淀粉样蛋白的药物研发。
 |
但现实很残酷。美国研究制药工业协会的统计显示,在截止2017年的20年里,各制药企业的治疗药开发项目为4胜146败。获得成功的只是以缓解症状为目的的药物,针对淀粉样蛋白的治疗药开发项目全部遭遇失败。
Aducanumab是使用蛋白质“抗体”(人类免疫的基础物质)的一种抗体药物。治疗对象为患有轻度认知障碍的患者。据说只清除脑部淀粉样蛋白块的设计发挥了成效。以往的失败药物的作用原理是阻碍脑部淀粉样蛋白的合成,或者清除溶解到血液中的淀粉样蛋白。
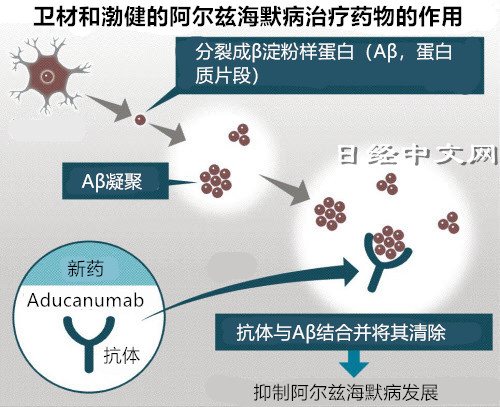 |
患者使用Aducanumab之后,抗体会与淀粉样蛋白块结合。与抗体结合的淀粉样蛋白块会被人类的免疫系统判定为异种物质,并被免疫细胞排除。
另一个成功因素是用药量。一般而言,大脑有防止异物侵入的屏障,药物成分难以到达。锭剂等分子量小的药物成分能到达,而分子量大的抗体药物基本到达不了。渤健(Biogen)和卫材选择了最大限度增加用药量的方法。
已证明通过送达用药量的0.几%,可以去除淀粉样蛋白斑块。普通抗癌药使用的抗体药物的用药量为体重1KG服用3~5毫克左右,Aducanumab为10毫克,是普通药物的2倍以上。
经过大约1年半的临床试验发现疾病进展速度可延缓2成,基本没有严重的副作用。实际上,以每月1次的频率通过点滴用药。
具有化时期的治疗效果,但科学界也有批判的声音。因为增加了用药量的患者人群具有抑制疾病进程的效果,但用药量少的患者人群没有明确的效果。部分专家也指出“评估效果用的数据不足”。
出乎意料获得批准
2020年11月,FDA邀请了外部专家召开的咨询委员会以科学依据不足为由,给出了不予批准的意见。也有人认为“Aducanumab不会获得批准了”(国内机构投资者)。
而FDA的判断出乎人们的意料。东京都健康长寿医疗中心的岩田淳部长表示“虽是附带条件批准的,但打开了开发治疗药物的大门”。
针对淀粉样蛋白斑块增加用药量的方法将成为今后开发治疗药物的方向。渤健和卫材的第2款治疗药物“Lecanemab”和瑞士罗氏的“Gantenerumab”正在做最终临床试验,2022年内出结果。美国礼来公司的“Donanemab”最近也将开始最终临床试验。有人指出美国也可能出现新药批准高峰。
Aducanumab在美国已于2020年8月作为优先审核对象受理申请,仅10个月就获批了。而在日本的审批还未通过,不过岩田认为“美国已批准的药物在日本很难被否定”。
日本经济新闻(中文版:日经中文网) 高田伦志
版权声明:日本经济新闻社版权所有,未经授权不得转载或部分复制,违者必究。
