新冠抗体治疗药在美国进入实用阶段
2020/11/24
在新冠治疗方面被视为首选药物的“抗体药物”已进入实用化阶段。美国企业正在开发的新药相继在美国国内附加条件获准使用。现在的新冠治疗药大多是转用其他疾病的治疗药,但抗体药物则是新冠专用药。与预计近期在局部启动接种的疫苗一起,抗体药物有可能开辟克服新冠病毒的道路。
抗体是与冠状病毒结合后使病毒失去活力的蛋白质,被用于抗体药物。模仿已康复者的血液中的抗体等,由人工制造。据称抗体药物主要面向轻症至中等程度的患者,通过早期用药,有望减少重症患者。
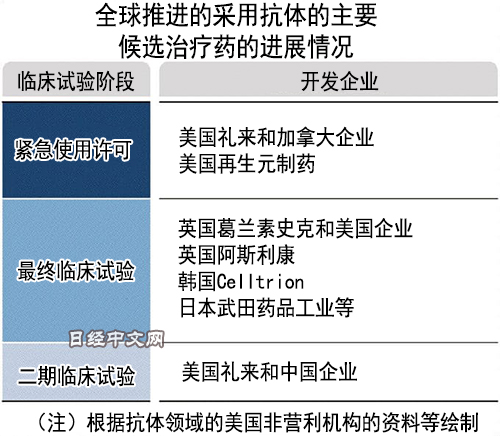 |
美国食品药品监督管理局(FDA)11月21日批准了美国再生元制药(Regeneron Pharmaceuticals)开发的抗体药物的紧急使用。这是美国总统特朗普感染新冠病毒时使用的药物,虽然仍未获得正式批准,但允许在没有其他有效治疗方法等情况下使用。
目前临床试验的结果显示,对并未住院的轻症到中等程度患者用药后,其体内的病毒量减少。FDA在声明中指出,“显示出(患者用药后)住院和急救治疗的减少”。
 |
| 美国药企礼来的标志(REUTERS) |
FDA在11月上旬向美国药企礼来(Eli Lilly)的抗体药物“Bamlanivimab”发出紧急使用许可。在该公司的第2阶段临床试验中,在用药的患者中,需要住院和进入重症监护室(ICU)的患者仅为1.6%,遏制了重症化。
日本岛根大学的浦野健教授表示,“如果能在较早阶段抑制体内病毒繁殖,很有可能减轻重症化风险”,指出了抗体药物的效果。
现在的新冠治疗药均为面向其他疾病开发出来的药物。作为代表性例子“瑞德西韦(Remdesivir)”原本面向埃博拉出血热而开发,抑制免疫失控的“地塞米松(Dexamethasone)”则面向风湿病等。
不过,这些药物的效果分化和使用困难等问题被指出。针对瑞德西韦,世界卫生组织(WHO)表示“不建议对住院患者使用”。而在日本,很多医生承认具有一定效果,但该药的评价在各国存在分歧。
抗体药物的开发将迅速推进。包括搁置的药品在内,全球现在有近20种候选药推进临床试验,数种药已进入最终阶段。另一方面,关于抗体药物临床试验的数据和评估仍未全部齐备,副作用也是未知数。获得紧急使用许可的2种也仍在推进最终临床试验,以进行验证。
另一个课题是成本。一般来说,抗体药物容易昂贵。虽然抗体药物在癌症治疗等方面得到使用,但按日本的药价计算,1次治疗需要数百万日元的情况很多。
即使作为新冠治疗药的效果得到认可,全球大量患者也可能无法承担抗体药物的费用。美国政府与礼来签署了3.75亿美元的合同,在处于紧急使用许可的期间,预计在无需患者自己负担费用的情况下提供药物。对于抗体药物的普及,预计有关用药对象患者等的讨论也必不可少。
版权声明:日本经济新闻社版权所有,未经授权不得转载或部分复制,违者必究。
