日本打造法匹拉韦国内供应链,规避海外风险
2020/07/23
日本富士胶片控股将构建供应链,以在日本国内稳定生产有望作为新冠治疗药的“法匹拉韦(favipiravir)”。作为原料厂商的电化(Denka)和钟化(Kaneka)等约15家企业给予协助,准备自9月起每月生产30万人份的法匹拉韦。日本从海外采购原料面临物流方面的风险,将转为国内采购。
法匹拉韦已作为新型流感药物获得批准,在日本政府完成储备的2018年之后停止生产。随着新冠疫情扩大,厚生劳动省提出复产请求,富士胶片于3月上旬恢复了生产。
 |
以前,法匹拉韦主要在中国采购原料进行加工,以医药“中间体”的形式进口到日本,经过制成药片等多道工序后成为药物。不过由于新冠疫情,出现了人员和物资的移动限制。富士胶片认为今后仍有可能发生物流混乱,判断原则上有必要在日本国内打造完整的供应链。
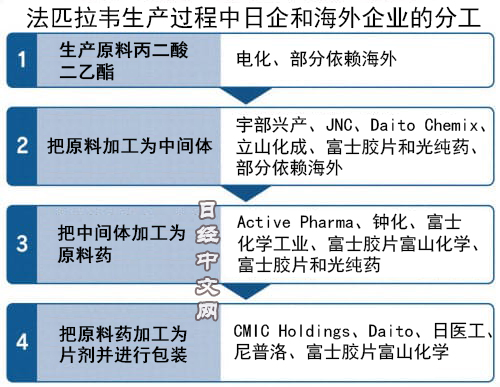
具体来说,约15家化学厂商和制药企业将围绕各工序进行分工。例如作为原料的丙二酸二乙酯,由电化(Denka)重启设备,自6月起供货。加工丙二酸二乙酯、制造中间体的工序由宇部兴产和立山化成负责。钟化和富士化学工业利用中间体制造作为有效成分的原料药。将原料药加工为药片的工序则由日医工和尼普洛(NIPRO)等提供协助。
 |
| 法匹拉韦 |
富士胶片将召集20~30名员工设置项目组,开拓供应商。此前,有些供应商的设备因生产其他产品而被占用,富士胶片就协助生产提出了请求。日本政府也为增强法匹拉韦的生产设备提供补贴,正在推动增产。这种药品此前无法全部在日本国内完成制造,今后将实现一条龙生产。
通过构建日本国内的采购网,富士胶片制订了7月生产10万人份、9月生产30万人份的时间表。此外,作为关联企业的FUJIFILM Wako Chemical将投入约10亿日元,提高原料药的产能。据称最快能自10月起增加10万人份的产量。
围绕新冠治疗药,日本在5月特例批准了美国药企吉利德科学(Gilead Sciences)的“瑞德西韦(Remdesivir)”。最近还批准了消炎药“地塞米松(Dexamethasone)”。法匹拉韦作为新冠治疗药正在实施临床试验,但未找到足够的志愿者,批准程序推迟。富士胶片将于7月内在科威特启动最多约1千人参与的大规模临床试验,力争在世界各国获得批准。
在富士胶片2020年度生产的约200万人份法匹拉韦中,日本政府不管是否获得批准,都将购买约130万人份作为储备。其余预计用于临床试验和海外销售等。
作为法匹拉韦主要成分的物质专利在日本仍然有效,但在海外很多国家已经到期。日本政府正向各国供应法匹拉韦,但供给量有限,因此海外出现了在本国生产仿制药的趋势。在中国、俄罗斯和印度,当地制药厂商生产仿制药,已获得批准。海外媒体报道显示,土耳其和埃及等国也出现生产法匹拉韦的动向。
一家制药企业的负责人表示,“由于新冠疫情,药品在安全保障方面受到关注,可能成为重要的核心技术”。不仅人员和货物的移动在空间上受到限制,在“有事”之际,各国将治疗药优先供应本国的可能性很高。不仅是法匹拉韦,包括人工呼吸机、防护服和口罩等在内,以本次疫情为契机,日本国内供应链的重要性出现提高。日本国内企业在生产方面开展合作的情况正在增加。
日本经济新闻(中文版:日经中文网)花田幸典
版权声明:日本经济新闻社版权所有,未经授权不得转载或部分复制,违者必究。
